Influência da Pressão Externa sobre o Ponto de Ebulição

O Ponto de Ebulição da água ao nível do mar é 100°C e a pressão atmosférica é de 100 000 Pa
É possível sim, depende somente da pressão externa. Mas, para entendermos como isso ocorre, vamos analisar primeiro o que é o ponto de ebulição (PE).

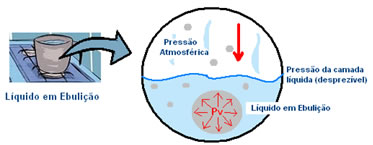
A pressão que o vapor exerce dentro da bolha é menor que a pressão externa, que é a pressão atmosférica, isto é, a pressão exercida sobre sua superfície. Porém, à medida que a temperatura vai aumentando, essa pressão de vapor (Pv) dentro da bolha também aumenta, até que ela se torne igual à pressão atmosférica e, por fim, entre em ebulição, ou seja, a bolha sobe para a superfície e é liberada no estado gasoso.
Outro ponto importante relacionado com isso é a altitude:
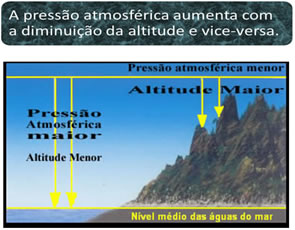
Se tentássemos fazer arroz no Monte Everest seria muito difícil, pois a água “secaria” antes do arroz cozinhar.
Agora, suponhamos fazer o contrário: ir para um lugar onde a altitude é menor que o nível do mar, como, por exemplo, o Mar Cáspio, um mar interior da Ásia, que tem altitude 28 metros abaixo do nível do mar. Nesse lugar, a água ferve a uma temperatura acima de 100°C.
Isso responde a pergunta que fizemos no início do texto. A água permanece no estado líquido a uma temperatura acima de 100°C, se a pressão externa for maior que a do nível do mar.
Por exemplo, a panela de pressão aumenta a pressão dentro de seu interior. O resultado será que o ponto de ebulição da água se elevará, ocorrendo por volta de 110 °C. Como ela permanece por mais tempo no estado líquido e mais quente, o cozimento dos alimentos será mais rápido.
Por Jennifer Rocha Vargas Fogaça

Nenhum comentário:
Postar um comentário